
اجزای شیمیایی یا ترکیب شیمیایی
اجزای شیمیایی چیست؟
اجزای شیمیایی یا ترکیب شیمیایی(chemical composition) هویت ، آرایش و نسبت عناصر شیمیایی تشکیل دهنده یک ترکیب را از طریق پیوندهای شیمیایی و اتمی مشخص می کند.
از فرمول های شیمیایی می توان برای توصیف مقادیر نسبی عناصر موجود در یک ترکیب استفاده کرد.
به عنوان مثال : فرمول شیمیایی متان CH4 است.
به این معنی که هر مولکول متان از 4 اتم هیدروژن (H) و 1 اتم کربن (C) تشکیل شده است.
ترکیب شیمیایی متان ممکن است به عنوان نسبت 4:1 اتم های هیدروژن به اتم های کربن تفسیر شود.
انواع مختلفی از فرمولهای شیمیایی برای انتقال اطلاعات ترکیب استفاده می شود، مانند فرمول تجربی یا مولکولی.
از نامگذاری می توان برای بیان نه تنها عناصر موجود در یک ترکیب ، بلکه آرایش آنها در داخل مولکولهای ترکیب استفاده کرد.
به این ترتیب و بر اساس نامگذاریهای اتحادیه بینالمللی شیمی محض و کاربردی(آیوپاک IUPAC) ، ترکیبات دارای نام های منحصر به فردی خواهند بود که می تواند ترکیب عنصری آنها را توصیف کند.
ترکیب شیمیایی یک مخلوط را می توان به عنوان توزیع مواد منفرد تشکیل دهنده مخلوط ، به نام "اجزا" تعریف کرد.
به عبارت دیگر، معادل کمی کردن غلظت هر جزء است.
از آنجایی که روش های مختلفی برای تعریف غلظت یک جزء وجود دارد ، روش های مختلفی نیز برای تعریف ترکیب یک مخلوط وجود دارد.
ممکن است به صورت کسر مولی , کسر حجمی , کسر جرمی , مولالیته , مولاریته یا نرمال بودن یا نسبت اختلاط بیان شود.
ترکیب شیمیایی یک مخلوط را می توان به صورت گرافیکی در نمودارهایی مانند نمودار سه تایی و نمودار چهارتایی نشان داد.

انواع پیوندهای شیمیایی :
پیوند کووالانسی:
پیوند کووالانسی یک نوع رایج پیوند است که در آن دو یا چند اتم الکترونهای ظرفیت را کم و بیش به طور مساوی به اشتراک میگذارند.
ساده ترین و رایج ترین نوع پیوند منفرد است که در آن دو اتم دو الکترون مشترک دارند.
انواع دیگر شامل پیوند دوگانه ، پیوند سه گانه ، پیوندهای یک و سه الکترونی ، پیوند دو الکترونی سه مرکزی و پیوند چهار الکترونی سه مرکزی است .
در پیوندهای کووالانسی غیر قطبی، اختلاف الکترونگاتیوی بین اتمهای پیوند خورده کوچک است ، معمولاً 0 تا 0.3
پیوندهای درون اکثر ترکیبات آلی به عنوان کووالانسی توصیف می شوند.
شکل متان (CH4 ) را نشان می دهد که در آن هر هیدروژن یک پیوند کووالانسی با کربن تشکیل می دهد.
مولکولهایی که عمدتاً از پیوندهای کووالانسی غیرقطبی تشکیل میشوند ، اغلب در آب یا سایر حلالهای قطبی غیرقابل اختلاط هستند ، اما در حلالهای غیرقطبی مانند هگزان بسیار حل میشوند.
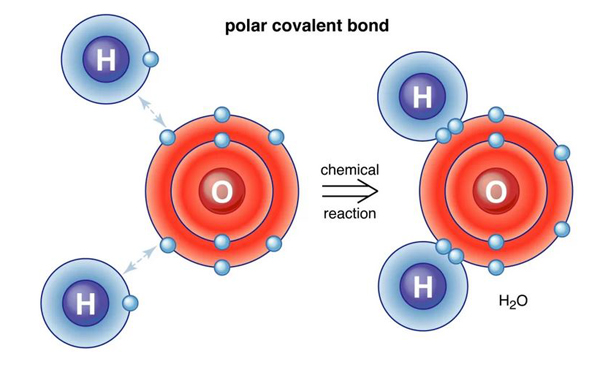
پیوند کووالانسی قطبی یک پیوند کووالانسی با ویژگی یونی قابل توجه است.
این بدان معنی است که دو الکترون مشترک به یکی از اتم ها نزدیکتر از دیگری هستند و باعث ایجاد عدم تعادل بار می شود.
چنین پیوندهایی بین دو اتم با الکترونگاتیوهای نسبتاً متفاوت ایجاد می شود و باعث برهمکنش دوقطبی-دوقطبی می شود.
اختلاف الکترونگاتیوی بین دو اتم در این پیوندها 0.3 تا 1.7 است.
پیوند یونی :
از ترکیب کاتیون با آنیون یک پیوند قوی به وجود می آید که به شکل نمک هستند.
پیوند یونی با انتقال الکترون همراه است یعنی یکی از اتمهای واکنش دهنده یک یا چند الکترون از دست میدهد و اتم دیگر یک یا چند الکترون میگیرد؛ و پیوند یونی، قویتر از پیوند هیدروژنی و واندروالسی است.
پیوند هیدروژنی :
اگر اتم هیدروژن در یک ترکیب شیمیایی به یکی از عناصر الکترونگاتیو با شعاع کوچک مانند نیتروژن ، اکسیژن و فلوئور متصل باشد ، دارای مقدار زیادی بار مثبت میشود که میتواند با همین اتمها در مولکولهای دیگر جاذبهای برقرار کند و نوعی نیروی بین مولکولی ایجاد نماید که به دلیل قدرت زیاد این نیرو به آن پیوند هیدروژنی می گویند.
معمولا این پیوند را با نقطهچین نمایش میدهند.
پیوند واندروالس :
حاصل نیروی جاذبه بین مولکولهای قطبی - قطبی ، قطبی - ناقطبی و نا قطبی- ناقطبی است ، مثل:
بین مولکولهای دو قطبی-دوقطبی=متانول و کلروفورم
بین مولکولهای ناقطبی تشکیل دو قطبی القایی (نیروی پراکندگی لاندن)=هگزان و اکتان
یون-دو قطبی=سدیم با آب
قطبی-ناقطبی=ید در اتانول
یون-دو قطبی القایی (بسیار ضعیف ونادر)
پیوند فلزی :
اگر ترکیب مورد نظر تنها شامل فلزات باشد، پیوند بین اتم های آن از نوع پیوند فلزی است.
کمپلکس شیمیایی :
از فلز و لیگاند تشکیل شده است.
ساختمان الکترونی این ترکیبات بستگی به نوع فلزها و آنیون های تشکیلدهندهٔ آنها دارد و میتوان با بررسی ساختار الکترونی اتمها آن را تعیین کرد.
نوع فلز و نیز نوع دو یا چند آنیون، مولکول خنثی و لیگاند که در این ترکیبات وجود دارد ساختمان آنها را تعیین میکند.
پیوند بین اتم ها از نوع پیوند داتیو است.
نکته مهم :
عناصر شیمیایی خالص ، در گروه ترکیبات شیمیایی قرار نمیگیرند ، حتی اگر از دو یا چند اتم از یک نوع عنصر (مثل S8 یا H2) تشکیل شده باشند که پیوندهای دو اتمی یا چند اتمی نامیده میشوند.
دسته فلزات و نافلزات:
نافلزات: اکسیژن. کربن. گوگرد و…
فلزات: آهن. مس. جیوه. طلا و…
تعریف و کاربرد فرمول شیمیایی :
شیمیدانها ترکیبهای شیمیایی را با بهکارگیری فرمولها توصیف میکنند.
شکلهای گوناگونی برای توصیف فرمول شیمیایی وجود دارد.
برای ترکیبهایی که به صورت مولکولی هستند، فرمول برای یک واحد مولکولی نشان داده میشود.
در مورد مواد پلیمری و دارای ساختارهای تکراری ، مانند مواد معدنی معمولاً فرمول تجربی مورد استفاده قرار میگیرد (مانند NaCl که فرمول تجربی نمک طعام است).
چینش نام عناصر در یک ترکیب شیمیایی با ترتیب مشخصی صورت میگیرد.
برای نمونه بر پایهٔ روشی که نامگذاری هیل نامیده میشود ، اگر اتمهای کربن و هیدروژن در یک ترکیب وجود داشتهباشند ، ابتدا کربن و پس از آن هیدروژن و سپس سایر عناصر به ترتیب الفبایی قرار داده میشوند.
یک روش دیگر آن است که عناصر به ترتیب الکترونخواهی خود در فرمول قرار داده میشوند.
در این روش ، ابتدا عناصر فلزی که کمترین الکترونخواهی را دارند در سمت چپ و عناصر غیر فلزی در سمت راست فرمول قرار میگیرند.
یک روش کامل تر، آن است که نوشتن فرمول با تکیه بر ساختار ترکیب انجام شود.
برای نمونه در ترکیبات آلی اسیدی، بخش آلی در سمت چپ و بخش اسیدی شامل COOH در سمت راست نوشته میشود.(برای نمونه، استیک اسید به صورت CH۳COOH نوشته میشود)
تفاوت ترکیب شیمیایی با مخلوط :
ویژگیهای فیزیکی و شیمیایی مخلوطی از چند عنصر یا ترکیب، مشابه با ویژگیهای مواد تشکیل دهندهٔ آنها است در حالی که ویژگیهای ترکیبها با عناصر تشکیلدهندهٔ آنها متفاوت است.
یک تفاوت معمول دیگر ترکیب با مخلوط آن است که میتوان مادههای تشکیل دهندهٔ یک مخلوط را با روشهای مکانیکی(مانند تبخیر و میدان مغناطیسی) به سادگی از یکدیگر جدا کرد ولی اجزای شکل دهندهٔ یک ترکیب تنها با استفاده از یک واکنش شیمیایی قابل تجزیه هستند.
برخی از مخلوطها مانند آلیاژهای فلزی، به گونهای با یکدیگر مخلوط میشوند که ویژگیهایی مانند ترکیبها پیدا میکنند.
ساخت ترکیب پایدار:
بسیاری از عناصر در حالت اتمی پایداری مناسبی ندارند و با یکدیگر ترکیب میشوند تا به حالت پایدارتر برسند.
آنها هنگامی به حالت پایدار میرسند که به بیشترین تعداد الکترون لایه ظرفیت و بیشترین سطح انرژی خود رسیده باشند که معمولاً تعداد ۲ یا ۸ ظرفیت الکترون است.
به همین دلیل گازهای نجیب غالباً واکنش نشان نمیدهند ، زیرا همهٔ ۸ الکترونهای ظرفیت آنها پر شده و نیاز به تغییر در ساختار الکترونی خود ندارند.(به جز هلیم که ۲ الکترون در لایه ظرفیت خود دارد).
همچنین ممکن است دو یا چند ترکیب که در مجاورت یکدیگر قرار دارند ، واکنش شیمیایی انجام داده و به یک یا چند ترکیب دیگر تبدیل شوند. برای نمونه ، هنگامی که یک باز و یک اسید با یکدیگر مخلوط شوند ، واکنش شیمیایی انجام داده و به یک نمک و آب تبدیل میشوند.
مانند ترکیب زیر:
NaOH+HCl➡️NaCl+H2O
فرآوردههای شیمیایی :
فرآوردههای شیمیایی به محصولاتی اطلاق میشود که از فرآیندهای شیمیایی تولید میشوند و معمولاً به عنوان مواد اولیه یا محصولات نهایی در صنایع مختلف استفاده میشوند.
این محصولات ممکن است به صورت مایع، جامد یا گاز باشند و از ترکیبات شیمیایی یا ترکیبات پیچیدهتر تشکیل شوند.
برخی از انواع فرآوردههای شیمیایی عبارتند از:
پلیمرها : موادی هستند که از تکرار واحدهای مولکولی کوچک به نام مونومرها ساخته شدهاند ، مانند پلاستیکها ، لاستیکها و فیبرهای مصنوعی.
کودها : موادی که برای بهبود کیفیت خاک و رشد گیاهان به کار میروند، مانند نیتروژن، فسفر و پتاسیم.
مواد شیمیایی حفاری : موادی که در فرآیندهای حفاری نفت و گاز به کار میروند، از جمله محلولهای حفاری و مواد شیمیایی جهت حفاری و گسترش چاه.
مواد شوینده و بهداشتی : محصولاتی که برای تمیزی و بهداشت استفاده میشوند، مانند صابون، شامپو و محصولات شستشو.
محصولات دارویی : فرآوردههایی که برای درمان بیماریها و بهبود وضعیت سلامتی استفاده میشوند، از جمله داروها و ویتامینها.
موارد اشاره شده تنها چند نمونه از فرآوردههای شیمیایی هستند و استفاده از آنها در صنایع مختلف به دلیل خصوصیات و خواص ویژه آنها بسیار گسترده است.
همچنین بخوانید :
درباره ما
شركت مينا تجهيز آريا با سالها تجربه و با استفاده از تخصص،تعهد، تجربه و دانش هاي نوين اقدام به تهيه، توزيع مواد شیمیایی ( آزمایشگاهی ، صنعتی ) و تجهيز لوازم آزمايشگاهي، شيشه آلات و كليه ملزومات آزمايشگاهي از شركت هاي داخل و خارج كشور نموده است.
برای پرسش و پاسخ و دریافت قیمت و موجودی با کلیک روی لینک زیر به تلگرام شرکت پیام دهید
آدرس : تهران - میدان توحید- خیابان امیر لو(نبش کوچه خودرو) - پلاک 42- طبقه دوم - واحد5
ایمیل : minatajhiz_aria@yahoo.com
شماره ها تماس : 02166901187 - 02166900058
شماره های همراه :09362048289 - 09927282910
شماره های واتس آپ ، ایتا ، تلگرام و روبیکا : 09927282910

